专家解读 | CHO重组表达产品上市申报前遗传稳定性研究要求
2024/12/18


赵清佳
微谱化药事业部毒理学研究专家
中国毒理学会认证毒理学家
赵清佳,微谱化药事业部毒理学研究专家,中国医药工业研究总院药物分析专业硕士,中国毒理学会认证毒理学家,深耕毒物分析技术开发与代谢机制研究领域。她拥有7年毒理学领域专业知识沉淀,含4年国内外药品及化学品毒理学风险评估实战经验,专注于为产品提供从研发到上市的全流程安全性合规解决方案。赵老师精通 ICH S 系列(药品)、OECD 测试指南、ECETOC TRA 及 REACH 等多国法规体系,能精准适配 NMPA、FDA、EMA等不同监管市场的合规要求,拥有丰富的产品申报/核查经验。

当已上市药品或申报品种中发现新的或水平升高的非致突变杂质,且其含量超过ICH Q3A/Q3B规定的界定阈值(QT)时,应如何进行科学、有效、合理的安全性评估?长期以来,行业普遍采用在原料药中“加样”该杂质,然后用此加样批次进行重复给药毒性动物实验。然而,该方法存在科学价值有限及违背3R伦理原则的 “双重困境”。

▲ 《关于非致突变杂质的界定的思考性文件》图源丨EMA官网
EMA《关于非致突变杂质的界定的思考性文件》的核心使命是为行业提供一套可替代传统动物实验、更具科学性和特异性的非临床安全评估策略,以填补ICH Q3A/Q3B在“超阈值新杂质或超限杂质”评估指导上的不足。该文件适用于化学合成原料药和制剂中的非致突变杂质,不适用于先进治疗药品、草药及生物制品。
针对上述问题,该文件构建了一套基于证据权重(Weight of Evidence,WoE)的风险评估决策流程图(见图1),其核心思想是:优先使用非动物方法(体内/体外毒理学数据、代谢物数据、交叉参照(Read-Across)以及NAMs(New approach methodologies)等进行安全性评估,仅在所有替代方法均无法解决安全隐患时,才考虑进行动物实验。
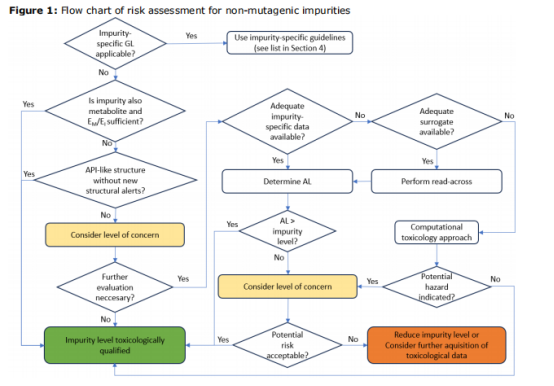
▲ 图1 基于证据权重(WoE)的风险评估决策流程
图源丨《关于非致突变杂质的界定的思考性文件》EMA官网
优先解决措施与建议如下:
1
代谢物法
如果该杂质在动物或人体的(非)临床研究中已被证实为代谢物,且其暴露水平(EM)与作为杂质摄入的预期暴露水平(EI)之比(EM/EI)足够高(通常≥1,对高风险代谢物需≥10),则可直接认定其安全性已被覆盖,无需额外数据。
2
Read-Across评估法
如果杂质本身不能查询出足够可靠的体外/体内毒性数据,可以根据其化学结构、物理化学性质、药代动力学等表征结果,采用单一替代或分组方法应用相似物的体外/体内毒性数据对该杂质进行安全性评估。
对于化学结构、理化性质与原料药高度相似,且未引入新的“警示结构”或“毒性基团”的杂质(如某些二聚体、水解/氧化产物),可认为其毒性特征已被原料药的毒理学研究充分覆盖。这与ICH M7中 “Class 4”杂质(与无致突变性的原料药具有相同警示结构)的逻辑一脉相承。
3
“关注水平”评估法
这是一个多因素综合判断过程,其关键考虑因素包括:
①最大每日摄入量:参考毒理学关注阈值(TTC) 概念。文件指出,虽然1.5 µg/天(源自ICH M7)是低关注起点,但1 mg/天常被用作一个重要的参考点:
摄入量低于TTC阈值则说明需关注度低;
介于TTC与1 mg/天之间则需个案评估;
高于1 mg/天则关注度显著升高。
②治疗时长:短于终生(LTL)暴露可允许更高的日摄入量,这与ICH M7中基于累积风险调整LTL限度的原则一致。
③患者人群:儿科、肝肾功能不全、孕妇等敏感人群需特别考虑。
④给药途径与临床适应症:严重或危及生命的疾病可容忍更高的风险。
此外,该文件详述了可接受水平(AL)计算方法论。如果关注水平评估认为需要进一步风险评估,则推荐计算AL。AL法借鉴了ICH Q3C(残留溶剂)和Q3D(元素杂质)中允许日暴露量(PDE) 的计算原理,但更具有灵活性。
关键评估起点(PoD):推荐优先使用基准剂量下限(BMDL),其次为未观察到的不良反应水平(NOAEL)等。
应用不确定因子(AFs):系统性地考虑了种属差异(AF1)、个体差异(AF2)、研究时长(AF3)、毒性严重程度(AF4)、LOAEL使用(AF5)、给药途径生物利用度差异(AF6)以及Read-Across评估的不确定性(AF7)。
产品特异性:可接受限度的计算公式为:AL(μg/d) = [PoD(mg/kg/d) × 50 kg × 1000] / (AF1 × AF2 × AF3 × AF4 × AF5 × AF6 × AF7)。
AL计算时需考虑特定药品使用背景,非通用限值。
4
NAMs
NAMs为当传统毒理学数据(如文献、交叉参照)不足时,用于支持非致突变杂质风险评估的补充性工具。其目的为在无需进行新的体内动物研究的情况下,填补特定的数据缺口,为杂质的危害识别或剂量反应评估提供证据。
①计算毒理学,应用符合OECD验证原则的(Q)SAR模型,识别警示结构、预测杂质的毒性效力;这与ICH M7要求使用两种互补的(Q)SAR方法进行致突变性预测的理念相呼应,但本文件将其扩展至非致突变性终点(如肝毒性、肾毒性等)。
②体外方法,使用细胞系、原代细胞、类器官或微生理系统等建立的体外测试模型,用于评估特定毒性终点、获取生物学数据;
③不良结局路径(AOPs),整合多源数据,构建从分子起始事件到不良反应的链条,用于定性或定量风险评估。
④危害表征与定量风险评估,若NAMs数据表明杂质对相关靶器官缺乏危害,此信息可作为证据权重的一部分,支持“风险可接受”的结论。若NAMs数据提示潜在危害,则评估者必须结合暴露水平、药代动力学考量及所有其他可用数据,进行综合判断,以论证在拟定质量标准限度下的暴露是否不存在安全风险。
最后,仅当上述所有方法均无法支持杂质在拟定标准下的安全性时,才考虑进行动物实验。文件对此提出了设计建议:必须使用纯度>95%的分离杂质,而非“加样”原料药,以确保观察到的效应确由杂质引起;推荐采用至少4个剂量组,以支持BMDL计算;纳入毒代动力学(TK)评估;遵循OECD测试指南等。
微谱拥有丰富的药品/化学品毒理评估项目经验、具备中国和美国毒理学家资质认证的技术团队。已为百余家客户提供了药物活性物质HBEL/PDE评估报告,助力客户通过药品共线生产清洁验证现场核查。微谱团队拥有近5000种非活性物质/杂质毒性数据库及Case Ultra基毒预测评估软件,致力于帮助客户解决杂质研究、香精成分小分子醛类物质等研究难题,助力企业顺利通过申报。
更多详情 · 请联系
电话:021-3178-5055
邮箱:yiyao-marketing@weipugroup.com